Captagon: la droga dell’ISIS
Il fenomeno delle nuove sostanze psicoattive continua a rappresentare una grossa sfida per la sanità pubblica. Benché nel 2016 siano pervenute al sistema di allerta rapido dell’UE segnalazioni di nuove sostanze al ritmo di una alla settimana, la cifra complessiva delle nuove sostanze scoperte è stata inferiore rispetto agli anni precedenti. Se tale flessione dovesse continuare, si tratterebbe di un segnale positivo. Tuttavia, vi sono anche altri dati meno incoraggianti che non sembrano puntare in direzione di un calo della disponibilità generale di nuove sostanze psicoattive. Inoltre, anche se il ritmo al quale vengono introdotte nuove sostanze sta rallentando, il numero complessivo delle sostanze disponibili sul mercato continua pur sempre a crescere (EMCDDA, 2017).
Tra le sostanze più comunemente riscontrate nel territorio europeo, troviamo gli psicostimolanti in particolar modo cocaina, amfetamina e i suoi derivati, il cui mercato e la cui produzione sono influenzati dalla presenza di precursori chimici (sostanze chimiche, anche destinate ad usi legittimi, essenziali per la loro sintesi).
I sequestri nel corso dell’ultimo decennio indicano che la disponibilità di metamfetamina è aumentata, pur rimanendo nettamente inferiore a quella dell’amfetamina. Entrambe queste sostanze vengono prodotte in Europa per uso interno. Vi sono indicazioni che la produzione di amfetamina avviene principalmente in Belgio, Paesi Bassi e Polonia e, in misura minore, negli Stati baltici, in Germania e Ungheria. La fase finale della produzione, vale a dire la trasformazione dell’olio dell’amfetamina base in benzedrina, sarebbe a sua volta situata in Europa. Una certa quantità di amfetamina è prodotta anche per essere esportata, soprattutto in Oceania e Medio ed Estremo Oriente. Di recente infatti sono anche aumentati i sequestri di compresse di amfetamina con il logo «Captagon», soprattutto in Turchia, dove nel 2015 ne sono stati confiscati più di 15 milioni (EMCDDA, 2017).
Oggi l’utilizzo delle amfetamine è condizionato dagli ultimi eventi storici (EMCDDA, 2011). Uno dei più significativi e recenti, è avvenuto il 13 novembre 2015 a Parigi, dove sono accaduti una serie di attentati terroristici, durante i quali sono state eseguite delle sparatorie e degli omicidi. È stato l’attentato che ha provocato una maggior mortalità in Francia dai tempi della Seconda Guerra Mondiale; lo Stato Islamico dell’Iraq e del Levante ha ammesso la sua responsabilità per questo attentato. I testimoni, hanno descritto che alcuni assassini del noto locale parigino “Bataclan”, sembravano degli “zombie” durante l’assedio. In seguito all’attentato infatti, sono state rinvenute nelle abitazioni degli attentatori delle siringhe contenenti una sostanza psicoattiva ed è stato ipotizzato che siano state usate proprio prima dell’attacco. La polizia francese sta indagando se l’ISIS abbia provocato la strage sotto l’effetto di sostanze psicoattive, considerate da alcuni “la pozione del terrorismo”, questo potrebbe spiegare la brutalità di questi attentati, in quanto possono facilitare atti di violenza estrema.
Il triste connubio: “uso di sostanze psicoattive e guerra”, non è di certo una novità, lo è diversamente l’utilizzo delle sostanze psicoattive in attentati terroristici, e visto che è stato riscontrato anche in altri successivi attentati, questo connubio ha dato origine al termine “Farmacoterrorismo”. Infatti, nell’attacco avvenuto sulla spiaggia della Tunisia nell’estate del 2015, è invece certo che il terrorista avesse assunto droghe psicoattive prima di iniziare la sua strage. Testimonianze riportano che lui stesse ridendo mentre sparava ed uccideva (Fond & Howes, 2016).
Il termine “Farmacoterrorismo” infatti può essere utilizzato per definire tutti quegli atti terroristici influenzati dall’uso di sostanze psicoattive, che inevitabilmente alterano, aumentano e precipitano la gravità di tali efferati attacchi (Khanra & Sen, 2016). È un fenomeno recentemente definito che sembra annoverare tra i suoi principali protagonisti proprio il “Captagon” la cui produzione sembra essere incrementata notevolmente in modo particolare in Siria, dove lo stato islamico dell’Iraq e del Levante è attivo (Fond and Howes, 2016; WCO, 2013).
Cos’è il Captagon?
 Dopo la sintesi dell’anfetamina nel 1887, primo psicostimolante sintetizzato, sono stati sintetizzati anche vari derivati sintetici, tra i quali si annovera il cloridrato di fenetillina (Al-Hussaini, 1996).
Dopo la sintesi dell’anfetamina nel 1887, primo psicostimolante sintetizzato, sono stati sintetizzati anche vari derivati sintetici, tra i quali si annovera il cloridrato di fenetillina (Al-Hussaini, 1996).
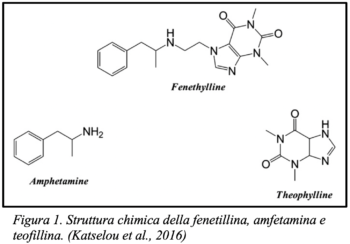
La fenetillina (nome IUPAC: 1,3-dimehtyl-7-[2-(1-phenylpropan-2-ylamino)ethyl]purine-2,6-dione), meglio nota come anfetaminoetilteofillina, anfetillina o con il nome arabo “Abu Hilalain”, è uno stimolante di tipo sintetico, nato dalla combinazione di amfetamina e teofillina, che si comporta come “profarmaco” di entrambe le sostanze psicoattive sopracitate.
Commercializzata con il nome di Captagon, Biocaptagon e Fitton, la fenetillina è diventata una delle sostanze illecite più utilizzate nel Medio Oriente (AL-Imam, 2016; Twark and Suzuki, 2017).
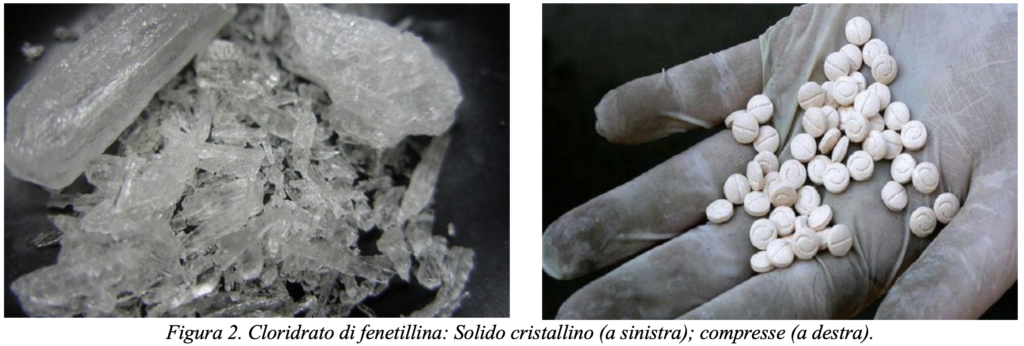
Il Captagon si presenta come un solido cristallino e la sua formula molecolare è C18H23N5O2, solitamente si trova come sale cloridrato nella formulazione di compresse (vedi fig. 2; Katselou et al., 2016).
La fenetillina fu sintetizzata per la prima volta nel 1961 da Chemiewerk Homburg, una filiale di Degussa AG, un’industria farmaceutica tedesca, grazie ad un programma di ricerca sugli effetti dei derivati della teofillina in particolar modo a carico dell’apparato cardiovascolare, respiratorio e sul Sistema Nervoso Centrale (SNC; Kristen et al., 1986; Ketselou et al., 2016).
Nonostante la Food and Drug Administration (FDA) non abbia mai approvato l’utilizzo clinico della fenetillina e quindi non fu mai commercializzata negli Stati Uniti, vi sono numerosi report di sequestri principalmente relativi a compresse di fenetillina contraffatte proprio negli USA (Kristen et al., 1986).
Diversamente invece, nella Repubblica Federale Tedesca, la fenetillina fu approvata e utilizzata dapprima senza obbligo di prescrizione (1961 – Aprile 1964) e poi come farmaco con obbligo di prescrizione (fino all’Ottobre del 1983) sotto forma di compresse da 50 mg, per la cura del disturbo del deficit dell’attenzione (ADHD) nei bambini, della narcolessia, epilessia e depressione (Kristen et al., 1986; AL-Imam et al., 2016). Uno dei vantaggi infatti dell’utilizzo della fenetillina, diversamente da altre anfetamine, era proprio quello di non alzare in modo significativo la pressione sanguigna (AL-Imam et al., 2016).
Nonostante sia attualmente una sostanza illegale, la fenetillina, è una delle sostanze d’abuso maggiormente riscontrate nei Paesi Arabi (presente tra i principi attivi delle compresse sequestrate e trafficate in Siria, con il nome di Captagon) e negli ultimi anni ha creato un particolare interesse perché utilizzata in particolar modo dai militanti di gruppi terroristici, per incrementare, similmente alle anfetamine, le performance e la resistenza fisica, nonché la resistenza e l’aggressività nel combattimento.
La fenetillina, nel corso degli anni fu illegalmente prodotta nell’Europa meridionale (Bulgaria, Slovenia, Serbia, Montenegro) e tutt’ora è rivenduta tramite la Turchia, ai consumatori della Penisola Araba. In base alle dichiarazioni riportate dall’UNODC, i tre paesi nei quali sono avvenuti più sequestri di Captagon, sono l’Arabia Saudita, la Giordania e la Siria. Quest’ultima, per molto tempo è stata un punto di transito per le droghe destinate alla Giordania, all’Iraq e al Golfo Persico, provenienti dall’Europa, dalla Turchia e dal Libano, come si evince dalla Fig. 3 sottostante (Katselou et al., 2016).
Le investigazioni anti-droga hanno scoperto che proprio da questo punto, il traffico di questa sostanza, si è espanso dalla Penisola Arabica fino all’Africa (Al-Imam et al., 2016).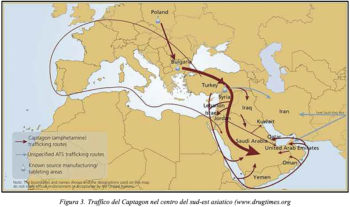
Le compresse di Captagon, vengono utilizzate dai gruppi militari in Siria, come l’ISIS e sono vendute ad un prezzo che varia tra i 3 e i 20 dollari, ma spesso anche barattate illegalmente, in cambio di armi (Katselou et al., 2016). L’evoluzione dell’uso del Captagon, in ambito politico-militare, è avvenuta quasi naturalmente: nel 2011, i manifestanti delle primavere arabe, confessavano di averlo ricevuto dagli organizzatori, per alimentare le manifestazioni di piazza; nel 2013 le Forze Armate Italiane inviate in Libia per arrestare i miliziani, riscontrarono che di questi, circa il 30% era dipendente dal Captagon; oggi i militari Curdi, assicurano di averla trovata in possesso dei militanti dell’ISIS, uccisi a Kobane (www.insostanza.it/droghe-guerre-captogon-isis/).
È fondamentale ricordare che Al-Qaeda ha appoggiato le leggi islamiche, per quanto riguarda l’uso e l’abuso di sostanze stupefacenti ed alcol; tali leggi, conosciute anche come “Sharia”, impongono ai mussulmani l’astenersi dal bere bevande alcoliche o dal fare uso di sostanze stupefacenti, escluse le sostanze ad uso medico e terapeutico. L’ISIS diversamente da Al-Qaeda, in relazione all’uso ed abuso di droghe, non ha aderito a queste leggi (Al-Imam et al., 2016).
Si sostiene che il Captagon sia utilizzato dai soldati dello Stato Islamico, per incoraggiarli ad andare a combattere, senza preoccuparsi di rimanere vivi o meno, proprio per i suoi effetti di inibizione della paura, rendendoli euforici ed impavidi, rendendo più sopportabile il dolore (in caso di ferite da arma da fuoco) e permettendo inoltre di combattere per un lungo periodo di tempo, dormendo poco, senza sentire la fatica e senza una diminuzione significativa della vigilanza (Van Hout & Wells, 2016).
Più di 1,4 milioni di compresse sono state sintetizzate in Siria e 107,5 kg in Turchia. Nel 2016 furono trovate 8,8 milioni di compresse, contenenti fenetillina in Egitto e 11.000 vicino alla capitale Irachena (Al-Imam et al., 2016).
Le indagini, che sono state fatte da una rivista americana, “Time and Reuters New Agency”, hanno rivelato che da quando l’economia all’interno del paese siriano è stata rallentata, a causa della guerra civile, le vendite di Captagon sono diventate la fonte principale delle entrate in Siria. Nel 2013, 12,3 milioni ci compresse di Captagon sono state sequestrate vicino al confine tra Libano e Siria. Nel 2014, 29,9 milioni sono state sequestrate a Dubai, altri 7 milioni invece sono state sequestrate nel tragitto tra la Siria e l’Arabia Saudita. Gli effetti del conflitto Siriano sull’Europa sono diventati sempre più significativi, non sono limitati solamente alle immigrazioni della popolazione araba, agli attacchi terroristici, che avvengono con molta frequenza negli ultimi anni, ma si stanno formando anche nuove vie per il commercio di questa droga (Van Hout & Wells, 2016). Il commercio online è una di queste ed è molto importante per la compravendita del Captagon, soprattutto nelle regioni toccate dai conflitti civili, Siria e Iraq, per prevenire tale commercio sono stati aumentati i controlli sui vari siti di acquisto come Amazon ed eBay; è significativo, che quando viene inserita nel motore di ricerca la parola “Captagon”, compare automaticamente un messaggio che avvisa che la ricerca è proibita. È stato rilevato che le ricerche provengono soprattutto dai paesi del Medio Oriente, prova del fatto che sono i maggiori trafficanti e consumatori. Il pagamento avviene attraverso il “Bitcoin Payments”, pagamento che permette di rendere anonima l’identità del compratore (Al-Imam et al., 2016; Katselou et al., 2016).
Aspetti farmaco-tossicologici
La fenetillina è storicamente oggetto di dibattito nel mondo scientifico, infatti, proprio la sua particolare struttura chimica, data dall’unione di una molecola di amfetamina e una di teofillina, divide il mondo scientifico, su quale sia il vero responsabile dei noti effetti psicoattivi. Alcuni studi infatti sostengono che sia proprio la fenitillina in sé (“parent compund”) ad avere degli effetti psicoattivi distinti da quelli indotti da altri psicostimolanti, altri studi invece sostengono che agisca semplicemente come profarmaco dell’amfetamina (Wenthur et al., 2017).
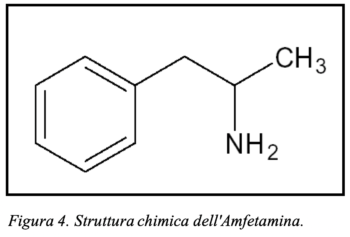
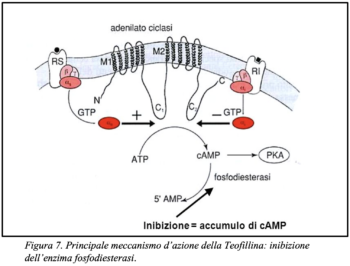
I più recenti studi scientifici circa gli aspetti farmaco-tossicologici della fenetillina, la considerano proprio come una sostanza distinta i cui effetti possono essere riconducibili ad un’azione sinergica tra i suoi due composti caratterizzanti: anfetamina (vedi fig. 4 e 5) e teofillina (vedi fig. 6 e 7; Nikel et al., 1986; Katselou et al., 2016; Wenthur et al., 2017).
Infatti, non solo i primi report clinici evidenziavano un minor potenziale d’abuso e un effetto trascurabile sulla pressione arteriosa e sull’appetito rispetto ad amfetamina e derivati (Kristen et al., 1986), ma anche un più recente studio preclinico pubblicato sulla prestigiosa rivista “Nature”, evidenzia come l’iperlocomozione indotta da fenetillina sia più rapida di quella indotta dalla somministrazione intraperitoneale di amfetamina nel modello murino (Wenthur et al., 2017).
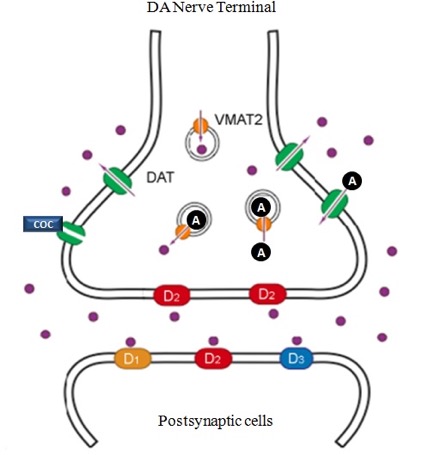
Figura 5. Immagine di una sinapsi dopaminergica dei rispettivi terminali pre e post sinaptici. Il VMAT2 immagazzina la dopamina nelle vescicole e il rilascio del neurotrasmettitore nella sinapsi permette il legame ai recettori dopaminergici: D1, D2 e D3. D2 localizzato anche nel terminale pre-sinaptico, agisce con un meccanismo di feedback nel regolare il rilascio di dopamina. I trasportatori della dopamina si trovano nei terminali pre-sinaptici fanno terminare l’azione della dopamina con un meccanismo di trasporto (re-uptake dal terminale pre-sinaptico). L’azione degli psicostimolanti sul DAT altera le normali funzione dei recettori dopaminergici. L’amfetamina (A) è un substrato del DAT, attraverso il quale entra nel citoplasma del terminale presinaptico dove agisce anche sul VMAT2, stimolando il rilascio di dopamina dalle vescicole citoplasmatiche, che viene poi riversata nella sinapsi attraverso l’azione invertita del DAT (Howell et al., 2008).
Osservazione coerentemente sostenuta anche dal fatto che la fenetillina è più lipofila di amfetamina e teofillina per questo raggiungerebbe più rapidamente il SNC ed esplicherebbe più velocemente l’attività psicostimolante (Nikel et al., 1986; Katselou et al., 2016).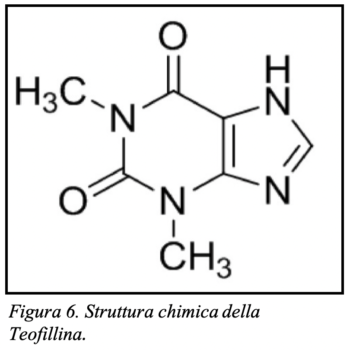
Tuttavia, Wenthur et al. sostengono invece che la penetrazione di amfetamina nel tessuto cerebrale, dopo somministrazion e di fenetillina, sia ritardata rispetto alla diretta somministrazione di amfetamina sostenendo inoltre che sia proprio quest’ultima disparità a potenziare ulteriormente la base farmacologica dell’attività psicostimolante.
Infatti la co-somministrazione di dosi inefficaci di teofillina e amfetamina potenzia la risposta locomotoria nel modello murino. Risposta osservata anche con altre combinazioni di derivati xantinici e fenetilamine, che si oppone alla precedente teoria secondo la quale, la concomitante liberazione di queste due diverse sostanze dovrebbe migliorare il profilo rischio/beneficio della fenetillina stessa (Wenthur et al., 2017). Queste considerazioni supportano in ogni caso l’emergere di una caratteristica esperienza stimolante soggettiva indotta dalla fenetillina, generata proprio dalla contemporanea alterazione del segnale adenosinergico e dopaminergico, fornendo così una spiegazione plausibile del significativo impegno da parte dei gruppi armati, nel cercare di addizionare ai prodotti contraffatti delle xantine, invece di produrre semplicemente delle sostanze amfetamino-simili (Wenthur et al., 2017).
Ulteriori studi farmacologici preclinici rivelano come la fenetillina somministrata per os, aumenti l’attività motoria nei topi dopo 90-120 min. analogamente a quanto riscontrato con amfetamina. Questi effetti permangono fino a 180 min. dopo il trattamento, mentre la durata d’azione dell’amfetamina si protrae fino a 240 min. similmente alla teofillina, supportando ancora una volta la teoria secondo la quale la fenetillina agisce con un meccanismo caratteristico diversamente dall’amfetamina (Katselou et al., 2016).
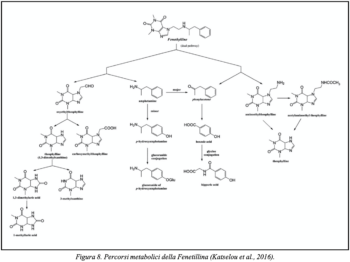 Il metabolismo della fenetillina, dopo la somministrazione orale, è complesso e segue due percorsi distinti (vedi fig. 8); oltre ai due metaboliti principali, quali l’amfetamina e la teofillina, si formano altri metaboliti secondari (Nikel et al., 1986). Nella prima via metabolica, la fenetillina viene ossidata, formando oxietilteofillina ed amfetamina. L’oxietilteofillina viene ulteriormente metabolizzata in teofillina dalla quale si formano i metaboliti finali: l’acido 1-3-dimetilurea, 3-metilxantina e l’acido 1-metilurico. Si forma solo una piccola quantità di teofillina libera, la carbossimetilteofillina. Nella seconda via metabolica si ha la formazione della 7-aminoetilteofillina e fenilacetone. Da questi si formano l’acido ippurico e la teofillina.
Il metabolismo della fenetillina, dopo la somministrazione orale, è complesso e segue due percorsi distinti (vedi fig. 8); oltre ai due metaboliti principali, quali l’amfetamina e la teofillina, si formano altri metaboliti secondari (Nikel et al., 1986). Nella prima via metabolica, la fenetillina viene ossidata, formando oxietilteofillina ed amfetamina. L’oxietilteofillina viene ulteriormente metabolizzata in teofillina dalla quale si formano i metaboliti finali: l’acido 1-3-dimetilurea, 3-metilxantina e l’acido 1-metilurico. Si forma solo una piccola quantità di teofillina libera, la carbossimetilteofillina. Nella seconda via metabolica si ha la formazione della 7-aminoetilteofillina e fenilacetone. Da questi si formano l’acido ippurico e la teofillina.
Infatti, dopo assunzione orale, dal metabolismo della fenitillina, si ottiene circa il 13.7% di teofillina (un blando psicostimolante simile alla caffeina) e circa il 24.5% di amfetamina (noto psicostimolante; Ellison et al., 1970). La formazione contemporanea di anfetamina e teofillina descrive la caratteristica farmacodinamica della fenetillina stessa (Ellison et al., 1970; Yoshimura et al., 1988).
Dal punto di vista farmacocinetico, la carbossimetilteofillina sembra escreta più velocemente rispetto all’amfetamina. Infatti, dopo 24-48 ore dall’assunzione orale di 30 mg di fenetillina, nelle urine si rilevano rispettivamente alti livelli di amfetamina, ma solo tracce di teofillina.
Proprio per la caratteristica breve emivita infatti, è spesso difficile individuare l’assunzione di fenetillina attraverso l’analisi delle urine e del sangue, risulta invece riscontrabile attraverso l’analisi del capello secondo una specifica metodica GC-MS (Yoshimura et al., 1988; Kikura and Nakahara, 1997).
L’effetto farmacologico della fenetillina è il risultato dell’azione combinata di questi due agenti psicostimolanti. Inoltre va ribadito che è molto più lipofila delle singole molecole di anfetamina e teofillina raggiungendo con ancora più facilità il Sistema Nervoso Centrale (principale target d’azione) nonostante il time-course degli effetti sia pressoché simile a quello dei due costituenti citati (Katselou et al., 2016).
La fenetillina stimola il sistema nervoso centrale, aumentando la vigilanza, la capacità di concentrazione e le prestazioni fisiche, grazie alla sua struttura anfetaminica e la sua somiglianza ai neurotrasmettitori: noradrenalina e dopamina. A dosi moderate, causa la dilatazione delle vene e delle arterie bronchiali ed aumenta la frequenza cardiaca e la pressione sanguigna. Tuttavia non incrementa la pressione sanguigna con la stessa efficacia dell’amfetamina. Questi effetti moderati sulla pressione, sono presumibilmente il risultato dell’effetto vasodilatatore indotto dalla teofillina e quello vasocostrittore dell’amfetamina (Katselou et al., 2016).
L’assunzione di Fenetillina crea uno stato emotivo ben bilanciato e non la tipica euforia associata alle sostanze di tipo amfetaminico (Janke & Boss, 1961). Ha un’azione anoressizzante minore, rispetto l’anfetamina e non interferisce con le normali attività motorie, ma migliora le prestazioni e tende a sviluppare meno dipendenza, rispetto l’anfetamina e ad altri psicostimolanti (Kristen et al., 1986). L’utilizzo della fenetillina, ha degli effetti diuretici e degli effetti nootropi positivi, simili a quelli che si hanno dopo l’assunzione di teofillina e diversi rispetto a quelli associati all’amfetamina (Daweke & Oberdorf, 1958; Yelnosky et al., 1962).
I primi studi scientifici suggerivano inizialmente, che la fenetillina si comportasse come profarmaco dell’amfetamina, ma le molteplici differenze tra le due singole sostanze, non sono coerenti con quest’ipotesi. La fenetillina evidenzia invece attività farmacologiche diverse, con minori effetti collaterali e un minor rischio d’abuso rispetto agli psicostimolanti amfetamino simili (Kristen et al., 1986; Katselou et al., 2016).
Tuttavia, l’uso prolungato del Captagon può presentare importanti effetti collaterali, tra i più comuni riportati dagli “User” ricordiamo: depressione, palpitazioni occasionali, malnutrizione, secchezza delle fauci, disturbi gastrici, crampi muscolari, vertigini e vista offuscata. Quelli meno riscontrati sono: sbalzi d’umore, confusione, rabbia improvvisa, irritabilità ed impazienza (Katselou et al., 2016).
Da evidenziare inoltre alcuni casi di infarto del miocardio. In particolare, si riporta il caso clinico di un ragazzo di 21 anni ricoverato al pronto soccorso dell’ospedale statale in Turchia nel 2012 in stato confusionale, con manifesti comportamenti aggressivi e un forte dolore al petto, dopo aver ingerito una compressa di Captagon. Il ragazzo, durante il monitoraggio cardiaco, che evidenziò una fibrillazione ventricolare, collassò e successivamente la coronarografia evidenziò una strozzatura a livello della porzione prossimale dell’arteria discendente anteriore sinistra (Uluçay et al., 2012).
Sintomi simili si possono sviluppare dopo il consumo di compresse di analoghi del Captagon. Infatti, anche se gli studi finora riportati in letteratura necessitano di ulteriori conferme, l’uso degli analoghi del Captagon, soprattutto tra i giovani consumatori, è stato correlato all’arresto cardiaco e a cardiomiopatia, (Uluçay et al., 2012; Katselou et al., 2016).
Analoghi del Captagon
Attualmente, in commercio, le compresse tradizionali di Captagon non sono disponibili (Uluçay et al., 2012), bensì, si possono trovare i cosiddetti analoghi del Captagon, o Captagon contraffatto, conosciuti con l’acronimo “CCT” (Counterfeit Captagon Tablet; Al-Hussaini, 1995; Katselou et al., 2016). Sono compresse contraffatte, ma aventi il marchio delle compresse tradizionali (Van Hout & Wells, 2016).
Con l’avanzamento della guerra civile in Siria e del terrorismo, la domanda di Captagon è aumentata sempre di più (Al-Imam et al., 2016) e per far fronte a questa richiesta, spesso si ricorre proprio agli analoghi che non contengono cloridrato di fenetillina, perché i suoi precursori, sono difficili da recuperare sul mercato clandestino (Van Hout & Wells, 2016). Inoltre con gli analoghi del Captagon è stato possibile potenziare l’attività, rispetto al Captagon tradizionale, in modo da facilitare gli atti di violenza, da parte di chi ne fa uso (Fond & Howes, 2016).
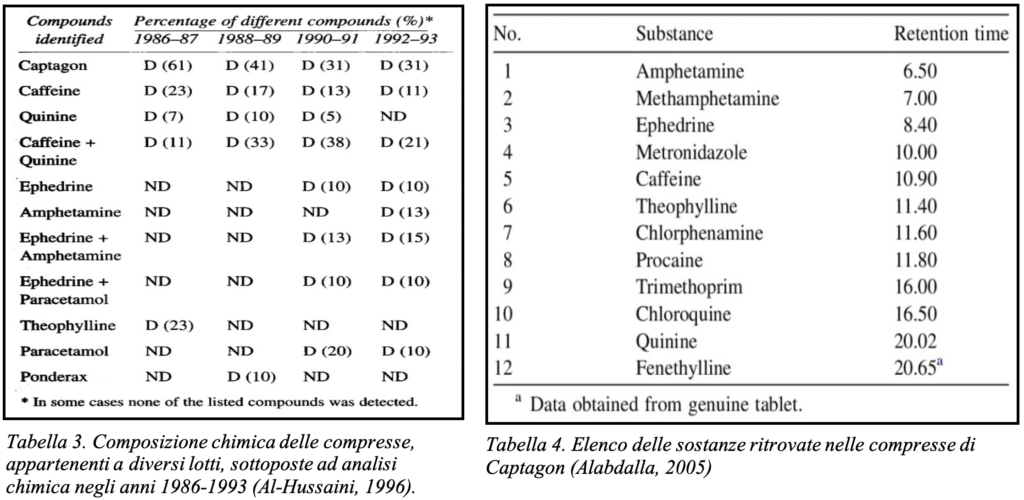
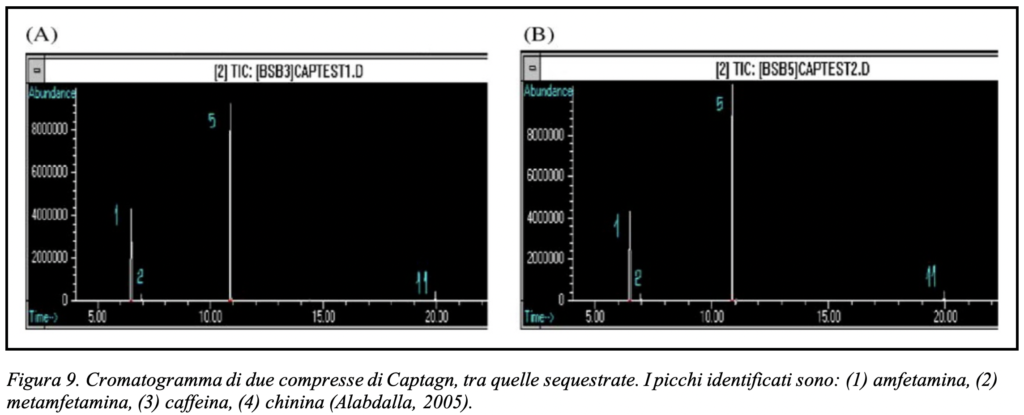
L’analisi chimica, delle compresse falsificate di Captagon, sequestrate tra il 1986 e il 1993 dalle autorità per il controllo delle sostanze stupefacenti dell’Arabia Saudita, ha evidenziato che diversi lotti differivano nella composizione chimica, e fisica dalle compresse tradizionali. L’esame fisico (vedi Tab. 2), ha evidenziato che tutte le compresse sequestrate avevano lo stesso diametro, ma con una durezza minore e uno spessore maggiore rispetto alle compresse tradizionali. Il colore inoltre differiva da quelle tradizionali, che erano bianche, mentre quelle falsificate erano o bianche o color panna.
L’esame chimico ha evidenziato che i campioni del gruppo delle compresse bianche, contenevano la fenetillina, la caffeina e la chinina; le compresse del gruppo color panna, al posto della fenetillina, contenevano altri composti, compresi i derivati dell’amfetamina, i dettagli delle sostanze trovate, sono riportate nella Tab. 3 (Al-Hussaini, 1996). Nel 2005 in Giordania furono sequestrate 124 dosi di Captagon contraffatto e attraverso l’analisi gascromatografica (GS-MS), si evidenziò non solo una notevole differenza di composizione tra le diverse compresse analizzate, ma anche che la maggior parte delle compresse conteneva sostanze in grado di indurre effetti simili a quelli della fenetillina, anche se quest’ultima era assente. Oltre all’anfetamina, metamfetamina e caffeina (vedi Tab. 4), le sostanze maggiormente riscontrate nelle compresse analizzate furono (Alabdalla, 2005): procaina (anestetico locale), che potrebbe spiegare l’effetto antidolorifico attribuito al CCT, ed efedrina (simpaticomimetico, che può aumentare gli effetti stimolanti degli analoghi del Captagon; Fond & Howes, 2016), paracetamolo (acetaminofene), chinina, metronidazolo, clorfenamina e altre sostante che possono causare sintomi gravi a livello cardiaco e non solo.
Legislazione e Conclusioni
La fenetillina è una sostanza inserita nella tabella I della lista delle sostanze controllate negli Stati Uniti dal 1981, dove non è attualmente approvata per uso medico (Katselou et al., 2016). Inoltre, nonostante l’incidenza d’uso del Captagon, sia abbastanza limitata, nel 1986 è divenuto illegale in molti paesi dopo l’inserimento da parte dell’Organizzazione Mondiale della Sanità nella lista internazionale delle sostanze psicotrope. Attualmente, risulta sotto controllo anche in Canada, Germania, Giordania e Italia (inserita in Tabella I delle Sostanze Stupefacenti e Psicotrope; http://www.salute.gov.it/imgs/C_17_pagineAree_3729_listaFile_itemName_0_file.pdf).
Da questo elaborato emerge come sia cambiato l’uso della Fenetillina, da farmaco a droga psicostimolante illegale. Tuttavia, pur essendo illegale è la sostanza psicostimolante più utilizzata dai ragazzi arabi benestanti, in età compresa tra i 12 e i 22 anni così come tra i soldati e combattenti jihadisti dell’ISIS (i sequestri in Siria nel 2015, accertano che i militanti dell’ISIS, facevano uso di questa sostanza; Van Hout & Wells, 2016; www.arabnews.com/saudi-arabia/news/826906; Katselou et al., 2016). Inoltre, secondo, il Comitato Nazionale per il Controllo delle Droghe delle Nazioni Unite, il Captagon è lo psicostimolante più diffuso, del gruppo delle anfetamine, nella Penisola Araba dove la Siria sembra essere il maggiore produttore, consumatore ed esportatore (Katselou et al., 2016).
Purtroppo, il commercio del Captagon è in aumento, non solo nel Medio Oriente, ma anche nell’Unione Europea dove un impulso molto importante è dato dall’e-commerce, che è strettamente legato alle organizzazioni terroristiche, come l’ISIS (Al-Imam et al., 2016). Inoltre, in questi ultimi anni, sul mercato nero sono apparsi analoghi del Captagon, ossia compresse contraffatte di Captagon “CCT” e queste vengono oggi maggiormente assunte dai terroristi dell’ISIS, prima dei loro atroci attacchi. Certamente l’utilizzo di questa droga non è la causa degli ultimi attacchi terroristici, ma è un nuovo capitolo dell’uso improprio delle droghe psicoattive definito con un termine ben preciso “Farmacoterrorismo” (Foun & Howes, 2016). Proprio per questo motivo, sono necessari ulteriori studi riguardanti il ruolo di questa droga negli attacchi terroristici e nelle zone di guerriglia nel Medio Oriente. Il Captagon usato dai terroristi dell’Isis, infatti è solo l’ultimo di una lunga serie di sostanze usate in guerra per togliere le inibizioni, sconfiggere la paura, sopportare la fatica e innalzare la soglia del dolore.
Bibliografia
Alabdalla MA., Chemical characterization of counterfeit captagon tablets seized in Jordan. Forensic Sci Int. 2005 Sep 10;152(2-3):185-8.
Al-Hussaini S.R., Department of Forensic Chemistry and Toxicology, Central Laboratory and Blood Bank, PO Box 56737, Riyadh-11564, Kingdom of Saudi Arabia. Science & Justice. 1996; 36:139-142.
Al-Imam A, Santacroce R, Roman-Urrestarazu A, Chilcott R, Bersani G, Martinotti G, Corazza O., Captagon: use and trade in the Middle East, Hum Psychopharmacol. 2016;32 (3).
Baskin-Sommer B, Sommer I., Methamphetamine use and violence among young adults, Journal of Criminal Justice. 2006; 34:661-674.
Berman S, O’ Neill J, Fears S, Bartzokis G, London ED., Abuse of Amphetamines and Structural Abnormalities in the Brain, 2008; Ann N Y Acad Sci. 2008 Oct;1141:195-220.
Cheng MH, Block E, Hu F, Cobanoglu MC, Sorkin A, Bahar I., Insight into the modulation of dopamine transporter function by amphetamine, ordrine, and cocaine binding, Frontiers in Neurology, 2015; 6:134.
Daweke H, Oberdorf A., Aminoalkyl derivatives of theophylline, Arzneimittelforschung. 1958 Apr;8(4):190-6.
Deree J, Martins JO, Melbostad H, Loomis WH, Coimbra R., Insights into the regulation of TNF-alpha production in human mononuclear cells: the effects of non-specific phosphodiesterase inhibition, Clinics (Sao Paulo). 2008 Jun;63(3):321-8.
Ellison T, Levy L, Bolger JW, Okun R., The metabolic fate of 3H-fenetylline in man, Eur J Pharmacol. 1970;13(1):123-8.
EMCDDA (European Monitoring Centre of Drugs and Drug Addictions). EU Amphetamine 2011.
EMCDDA (European Monitoring Centre of Drug and Drug Addiction). EU Synthetic drug production 2015.
EMCDDA (European Monitoring Centre of Drug and Drug Addiction) 2017. http://www.emcdda.europa.eu/system/files/publications/4541/TDAT17001ITN.pdf
Essayan DM., Cyclic nucleotide phosphodiesterases, J Allergy Clin Immunol. 2001 Nov;108(5):671-80.
Fond G, Howes O., Pharmacoterrorism: the potential role of psychoactive drugs in the Paris and Tunisian attacks, Psychopharmacology (Berl). 2016 Mar;233(6):933-5.
Hart SP., Should aminophylline be abandoned in the treatment of acute asthma in adults?, QJM. 2000 Nov;93(11):761-5.
Howell LL, Kimmel HL., Monoamine transporters and psychostimulant addictions, Biochemical Pharmacology, 2008; 75: 196-217.
ISS (Istituto Superiore di Sanità) 2017. http://www.politicheantidroga.gov.it/media/2153/relazione-al-parlamento_2017.pdf
Janke W., Boss H., Experimental studies on the psychic effects of a new psychotonic drug, Arzneimittelforschung. 1961 Aug; 11:783-7.
Katselou M, Papoutsis I, Nikolaou P, Qammaz S, Spiliopoulou C, Athanaselis S., Fenethylline (Captagon) Abuse – Local Problems from an Old Drug Become Universal, Basic Clin Pharmacol Toxicol. 2016 Aug;119(2):133-40.
Khanra S, Sen S., Pharmacoterrorism: We should be worried, Asian J Psychiatr. 2016; 22:83.
Kikura R, Nakahara Y., Hair analysis for drugs of abuse. XVI. Disposition of fenethylline and its metabolite into hair and discrimination between fenethylline use and amphetamine use by hair analysis, J Anal Toxicol. 1997 Jul-Aug;21(4):291-6.
Kristen G, Schaefer A, von Schlichtegroll A., Fenetylline: therapeutic use, misuse and/or abuse, Drug Alcohol Depend, 1986 Jun;17(2-3):259-71.
Marques LJ, Zheng L, Poulakis N, Guzman J, Costabel U., Pentoxifylline inhibits TNF-alpha production from human alveolar macrophages, Am J Respir Crit Care Med, 1999 Feb;159(2):508-11.
Miczek KA, Nikulina EM., Takahashi A., Covington III HE, Yap JJ, Boyson CO, Shimamoto A., de Almeida RMM., Gene expression in aminergic and peptidergic cells during aggression and defeat: relevance to violence, depression and drug abuse, Behav Genet 2011; 41:787-802.
Miliano C, Serpelloni G, Rimondo C, Mereu M, Marti M, De Luca MA., Neuropharmacology of New Psychoactive Substances (NPS): Focus on the Rewarding and Reinforcing Properties of Cannabimimetics and Amphetamine-Like Stimulants, Front Neurosci. 2016 Apr 19; 10:153.
Murray JB., Psychophysiological Aspects of Amphetamines-Methamphetamines Abuse, The Journal of Psychology. 1998; 132,227-237.
Nickel B, Niebch G, Peter G, von Schlichtegroll A, Tibes U., Fenetylline: new results on pharmacology, metabolism and kinetics, Drug Alcohol Depend. 1986 Jun;17(2-3):235-57.
OEDT-Osservatorio Europeo delle Droghe e delle Tossicodipendenze. Consiglio dell’Unione Europea. Bruxelles, 2011.
Peters-Golden M, Canetti C, Mancuso P, Coffey MJ., Leukotrienes: underappreciated mediators of innate immune responses, J Immunol. 2005 Jan 15;174(2):589-94.
Shively CA, Tarka SM Jr., Methylxanthine composition and consumption patterns of cocoa and chocolate products, Prog Clin Biol Res. 1984;158:149-78.
Twark C and Suzuki J., Fenethylline-Induced Psychosis, Fenethylline-Themed Paranoid Delusions, or Both?, Psychosomatics. 2017 Sep-Oct;58(5):561-564.
Uluçay A, Arpacık Kargı C, Aksoy MF., Acute myocardial infarction associated with Captagon use, Anadolu Kardiyol Derg. 2012 Mar;12(2):182-5.
Van Hout MC, Wells J., Is Captagon (fenethylline) helping to fuel the Syrian conflict?, Addiction. 2016 Apr;111(4):748-9.
Welter-Luedeke J, Maurer M and H, PhD., New Psychoactive Substances: Chemistry, Pharmacology, Metabolism and detectability of amphetamine derivatives with modified ring System, Ther Drug Monit. 2016 Feb;38(1):4-11.
Wenthur CJ, Zhou B, Janda KD., Vaccine-driven pharmacodynamic dissection and mitigation of fenethylline psychoactivity, Nature, 2017 Aug 24;548(7668):476-479.
World Customs Organization, 2013. Illicit Trade Report 2013. http://www.wcoomd.org/-/media/wco/public/global/pdf/topics/enforcement-and-compliance/activities-and-programmes/illicit-trade-report/illicit-2013-_-en_lr2.pdf?db=web
Yelnosky J, Kirkpatrick GV, Govier WM., The cardiovascular actions of 7-(N-beta-methylphenethylaminoethyl) theophylline hydrochloride, J Pharmacol Exp Ther. 1962 Jun;136:318-26.
Yoshimura H, Yoshimitsu T, Yamada H, Koga N, Oguri K., Metabolic fate of fenetylline in rat and man, Xenobiotica. 1988 Aug;18(8):929-40.
Sitografia
www.arabnews.com/saudi-arabia/news/826906
www.insostanza.it/droghe-guerre-captogon-isis/
http://www.salute.gov.it/imgs/C_17_pagineAree_3729_listaFile_itemName_0_file.pdf